▲ Bourse minéraux et fossiles de Sainte Marie aux Mines (Alsace) - 25>29 juin 2025 ▲ |
-
Compteur de contenus
2616 -
Inscription
-
Dernière visite
Type de contenu
Profils
Forums
Galerie
Blogs
Boutique
Tout ce qui a été posté par Lionel-R
-

L'améthyste dans le monde
Lionel-R a répondu à un sujet de le sablais dans Forum Minéraux et Minéralogie
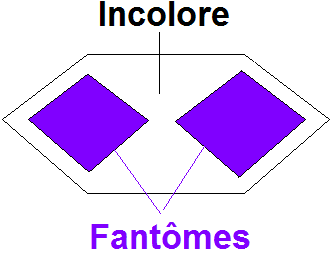
En fait non... il n'a pas cette forme, c'est à cette forme que je me serai attendu mais c'est complètement autre chose. Je joins un croquis qui explique mieux : Voila à quoi ça ressemble... C'est bizarre non ? Les cristaux de cet endroit ne sont pas tous comme ça, mais il y en a pas mal avec ces doubles fantômes. On en voit d'autres sur mindat dans les liens suivants : Lien 1 Lien 2 Lien 3 Lien 4 -

Boules de ?? dans cubes de fluorine
Lionel-R a répondu à un sujet de GEOLMANIA21 dans Demandes d' identification de minéraux
C'est vraiment très intéressant ton témoignage et même très déroutant pour deux raisons, la première je l'ai déjà exposée plus haut avec le potentiel du cuivre, la deuxième est ton expérience. Normalement en rajoutant une base tu devrais obtenir un hydroxyde de cuivre bleuté, un peu comme la chrysocolle, mais tu obtiens un métal rouge... est-ce qu'il devient vert après exposition à l'air humide ? Après l'eau de javel en plus d'être basique est un oxydant, après tout dépend des niveaux rédox si le cuivre est bien placé l'eau de javel peut faire office de réducteur, je n'ai pas vérifié. Il y a une autre façon de tester le cuivre qui est plus "orthodoxe", il suffit de plonger du fer (ou de l'acier) dans la solution bleue, le cuivre doit former un dépôt rouge sur le fer. Ce test est vraiment très caractéristique. Je vais faire l'expérience, parce que je suis vraiment très étonné par tout ça. Je te dirai par MP ce que j'ai pour ne pas alourdir le post. Merci encore ! -

L'améthyste dans le monde
Lionel-R a répondu à un sujet de le sablais dans Forum Minéraux et Minéralogie
Pas mal dis donc très intéressant. mais ça vient d'où plus précisément ? Les brandberg que je connais sont associés à l'analcime, épidote, phrénite et calcite. Je n'en ai jamais vu avec de l'orthose... Tu pourrais préciser la localité si tu en sais plus ? Ça mériterait des photos en lumière naturelle, pour mieux faire ressortir le violet, ne soit pas avare d'autres photos juste pour le plaisir !!! -
Pour avoir une idée de ce que pourrait être cette impureté, tout d'abords dissoudre ton carbonate dans HCl (dans un minimum d'acide !!!). Observe la couleur et prend une photo. Ensuite tu rajoute de la soude jusqu'à formation d'un précipité (prends une photo). Une fois ce précipité formé, tu dilue ta solution avec un peu d'eau pour dissoudre les grains de NaCl qui peuvent se former. S'il n'y a aucun précipité insoluble, rajoute de la soude jusqu'à formation d'un précipité. Si tu obtiens un précipité ocre-jaune, c'est du fer (FeOOH ou Fe2O3.nH2O ou autre), si tu obtiens un précipité plutôt noir, c'est du manganèse (MnOOH ou autre). Bien entendu tu prendras encore une photo. Il est utile d'être attentif à toutes les transformations qui ont lieu lors des expériences (couleur, effervescence, dégagement de chaleur etc....) tout ce qui peut être observé est important :) Après il est probable que ton impureté soit si peu concentrée qu'il ne se passe rien du tout.
-
Mais c'est super tout ça !!! rien de ridicule que du plaisir :)
-

Barytine ou fluorine...???
Lionel-R a répondu à un sujet de lemorvandiau dans Demandes d' identification de minéraux
Je vote fluo pour tout sauf pour la dernière photo ou comme les autres je vote baryte... -
C'est sur que la nature fait rarement des espèces bien pures, qu'on peut mettre plein de chose à la place du calcium mais ça vaut le coup d'essayer, sait on jamais. La teinte marron des échantillons suggère la présence d'une impureté !!! Sans être schizophrène, je suis persuadé que ça ne marchera pas (^^) mais on ne sait jamais !!! et puis c'est plus rigoureux qu'une analyse à l'œil. Les clivages peuvent aider aussi, tous parfait pour la calcite et pas pour l'aragonite (de mémoire)...
-
Mais très sérieusement cette attribution "aragonite" est basée sur des données bibliographiques ou c'est une analyse à l'oeil ? Si tu as une balance très précise tu peux mesurer la densité, celle de l'aragonite est de l'ordre de 2.94 contre 2.71 pour la calcite, c'est vraiment très proche, mais avec une masse de 20-25g et une balance à 0.1g près tu es assez précis, le must serait une balance à 0.01g près, là t'es tranquille, ne pas oublier de multiplier les mesures pour avoir une valeur plus proche de la réalité. Après corrigez moi si ce n'est pas possible de les différencier aussi simplement avec des moyens d'amateurs...
-

Quartz or not quartz ???
Lionel-R a répondu à un sujet de lemorvandiau dans Demandes d' identification de minéraux
Eh bien je veux bien dire que je ne suis pas convaincu par le quartz du fait de la terminaison et puis la section aussi... -

Boules de ?? dans cubes de fluorine
Lionel-R a répondu à un sujet de GEOLMANIA21 dans Demandes d' identification de minéraux
Tiens c'est marrant ça... c'est très surprenant car ça ne devrait pas être possible. Pour dissoudre le cuivre il faut l'oxyder et le potentiel standard du couple Cu/Cu2+ en permet pas son oxydation par H+... il faut une espèce oxydante et les nitrates de l'acide nitrique jouent ce rôle. C'est d'autant plus étrange que l'acide du vinaigre est un acide faible et peu concentré... c'est vraiment bizarre vu que l'acide sulfurique et l'acide chlorhydrique ne dissolvent pas le cuivre (sauf à chaud ou aidé par l'eau oxygénée). Vraiment je suis très surpris et très content de me coucher moins bête et avec une question à poser à mes collègues parce que c'est vraiment bizarre. Je ferai l'expérience !!! Merci Stalker (je n'ai pas d'idée pour faire cristalliser ton produit plus facilement, je te dirai si j'y arrive) PS : les majuscules ça veut dire que tu cries ! -
Chouette ça dis donc !!!! j'imagine l'horreur du transport et le stress après être rentré à la maison à l'ouverture du paquet... C'est sur ce que c'est de l'aragonite ?
-

Vous connaissez ce minéral ?
Lionel-R a répondu à un sujet de hallbopp dans Demandes d' identification de minéraux
Et sinon pour ceux qui ont la flemme de tout lire "une brèche sédimentaire à éléments anguleux ou arrondis de quartz, englobés dans une matrice ferrugineuse qui confère à la roche cette couleur rouge, brune ou jaunâtre si particulière. Ses gisements sont limités à la ville actuelle de Rennes. Il date certainement du Cénozoïque, vraisemblablement de l’Eocène, sa genèse étant liée à des silicifications sous le climat tropical qui régnait en Bretagne à cette époque." Voila ce qu'ils en disent, c'est quand même mieux que "caillou de rennes" -

Vous connaissez ce minéral ?
Lionel-R a répondu à un sujet de hallbopp dans Demandes d' identification de minéraux
Le caillou de rennes ? tu as trouvé ça ou ? -

Vos découvertes de minéraux les plus récentes
Lionel-R a répondu à un sujet de lionel63 dans Forum Minéraux et Minéralogie
Merci :) -

Vos découvertes de minéraux les plus récentes
Lionel-R a répondu à un sujet de lionel63 dans Forum Minéraux et Minéralogie
C'est vrai que c'est sympa, mais en "gros" ça vient d'où ? -

Découvertes minéralogiques mondiales
Lionel-R a répondu à un sujet de mineralparangon dans Forum Minéraux et Minéralogie
Non mais ça ne va pas de poster des choses comme ça ?! Punaise, ça pique les yeux... quand je pense en avoir une de cet endroit, je la savais pas terrible, elle est en fait vraiment très pourrie après ce que j'ai vu... démoralisé je suis :'( Pour la peine : http://www.coromotominerals.com un peu de pegmatite du Mont Micas (si je me rappelle bien). Comme tout à l'heure toujours miné dans la finesse quoi que cette fois il y des explosifs en plus des pelles mécaniques et autres marteaux piqueurs. Je ne connais pas la montagne noire, enfin je l'ai vu de loin et tout de même je la préfère telle qu'elle est, avec les explosifs et les pelles mécaniques... limite niveau "cocologique" non ? enfin bon pas la peine de lancer ce débat ici, continuons sur le mondial. -

Vos minéraux des Hautes-Alpes
Lionel-R a répondu à un sujet de tenola dans Forum Minéraux et Minéralogie
En terme de combinaison, on peut toujours imaginer la présence de cuivre II en site octaédrique dans la calcite. Ce n'est pas choquant dans la mesure ou on peut substituer (en faible quantité) le cobalt, le nickel, le manganèse et le magnésium au calcium. Sans vouloir semer le doute, sur un site totalement différent (dans l'Aude, tout près de Villeneuve-Minervois et Caprespine) je suis tombé sur des calcites associées vraisemblablement à de la chalcopyrite micro et présentant des zones vertes. Toutes les conditions semblaient réunies pour accuser le cuivre, mais une analyse à montré l'absence complète de cuivre et ce même à l'état de trace. Cela ne veut pas dire que les calcites présentées ne sont pas teintées par du cuivre surtout si des caractérisations poussées ont été effectuées, disons juste que le cuivre n'est pas toujours la bonne raison d'une coloration verte. L'affirmer sans l'avoir testé ou sans appui bibliographique précis peut être erroné. Par ailleurs, je ne sais toujours pas pourquoi mes calcites sont vertes. -

Boules de ?? dans cubes de fluorine
Lionel-R a répondu à un sujet de GEOLMANIA21 dans Demandes d' identification de minéraux
Très jolie ces petites boules, on dirait vraiment du cuivre. Si tu pouvais en récolter, le cuivre donne une couleur bleue dans l'acide nitrique (le acide seul capable de le dissoudre, hormis la dangereuse eau régale qui dissout presque tout). La dissolution s'accompagne de vapeur rousses de NOx toxiques, il n'y en aura pas beaucoup mais il faut éviter de les respirer. Est ce que tu peux zoomer sur les agrégats pour avoir plus de détails ? -

Vos découvertes de minéraux les plus récentes
Lionel-R a répondu à un sujet de lionel63 dans Forum Minéraux et Minéralogie
Moi j'ai trois questions pour les trois post qui précèdent le mien : Ça fait quelle taille ? Ça vient d'où ? (pas besoin de coordonnées GPS, une commune ou un coin de France me suffit largement, juste de quoi me faire une idée) Quels sont les minéraux du post qui précédant ma réponse ? -

Minéraux, mes dernières acquisitions...
Lionel-R a répondu à un sujet de pegasus dans Forum Minéraux et Minéralogie
Sacrilège ?! mais pourquoi le monde n'est pas français ^^ Et puis c'est esthétique tout ça ! Elle fait quelle taille cette pyromorphite ? -
Nozels si tu veux vraiment savoir d'ou pourrait venir ton cailloux il faut que tu postes des photos globales de la pièces, des détails des cubes et des photos de la gangue.
-
Courant je ne sais pas, mais à Huaron (Pérou) le quartz et la pyrite sont très souvent associés avec l'un sur l'autre ou inversement. On rencontre le même phénomène avec la chalcopyrite et la tétraédrite. En France ça doit se trouver aussi, mais je ne connais pas. Il me semble que les gisements de pyrite d'Argentine peuvent fournir du quartz sur de la pyrite mais là il faudrait vraiment vérifier. Niveau provenance je ne sais pas, je ne suis pas convaincu par Salsigne... mais bien loin d'être un spécialiste !
-

Vos découvertes de minéraux les plus récentes
Lionel-R a répondu à un sujet de lionel63 dans Forum Minéraux et Minéralogie
Mais t'es pas à Madagascar toi normalement ?! enfin bon si c'est pour nous montrer des choses comme ça :) allez gratte gratte !!! -

Vos découvertes de minéraux les plus récentes
Lionel-R a répondu à un sujet de lionel63 dans Forum Minéraux et Minéralogie
Vivement le nettoyage Augustin !!! -
Je te propose une couche gemme fracturée qui recoupe un grenat très opaque d'où l'aspect alvéolée. Après reste à savoir si c'est possible ou mieux : connu !